Secondo un recente studio lo Aztreonam lisina, un antibiotico inalatorio avente come target specifico Pseudomonas aeruginosa, è in grado di stabilizzare la funzione polmonare
Aztreonam lisina


Secondo un recente studio lo Aztreonam lisina, un antibiotico inalatorio avente come target specifico Pseudomonas aeruginosa, è in grado di stabilizzare la funzione polmonare



La missione di Danone è portare la salute attraverso l’alimentazione al maggior numero di persone possibili. Questo vale sia per chi è in salute, sia per chi non lo è.
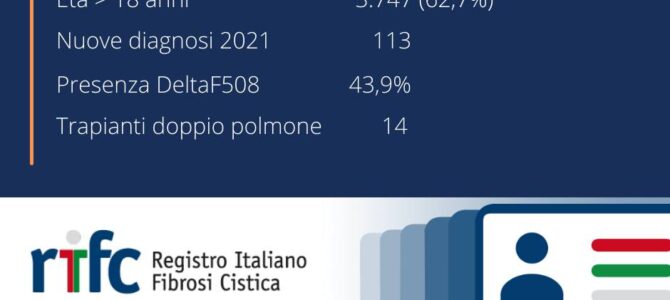
Il Registro Italiano Fibrosi Cistica ha pubblicato come ogni anno un report sintetico, ad uso dei pazienti, per segnalare i dati più significativi sullo stato della popolazione FC italiana. I dati sono stati trasmessi da 27 centri (per il 2021 mancano i dati…
L’impiego della terapia tripla di modulazione della proteina CFTR elexacaftor/tezacaftor/ivacaftor nei pazienti con fibrosi cistica (FC), sarebbe in grado anche di alleviare la sintomatologia sinonasale frequentemente associata. Queste le conclusioni di uno studio tedesco recentemente pubblicato sulla rivista European Archives of Oto-Rhino-Laryngology. Razionale e disegno dello…

Ringraziamo la Dott.ssa Paola Melotti e il Dott. Valentino Bezzerri per aver redatto e condiviso questa relazione. ‘Non lasciare nessuno senza cura per ogni difetto di base’ è stato il sentire comune di questo Congresso: una speranza che anche noi come comunità di pazienti…